link til prezi om ethanol et alkohol: http://prezi.com/iljqfe9yp5ye/?utm_campaign=share&utm_medium=copy&rc=ex0share
Ethanol et alkohol
Formlen for Ethanol er C2H5OH
Når endelsen er OH i den kemiske benævnelse så er det et alkohol.
Molekyler, hvor der indgår carbonatomer defineres som organiske forbindelser. Der er dog 2 undtagelser CO2 og CO, fordi de er uorganiske.
· Ethanol er en farveløs væske,
· Kogepunkt=78 grader,
· Frysepunkt=-117 grader
· Massefylden= 0,795 g/ml
Når ethanol brænder forekommer en fuldstændig forbrænding.
Afstemmes:
CO2H5OH+3Oà2CO2+3H20
Vand og kuldioxid kan ikke brænde derfor defineres det som en fuldstændig forbrænding.
Ånding er også en fuldstændig forbrænding (der dannes vand og kuldioxid)
Ånding er: Respiration og fotosyntese.
Kalkvand-Ca(OH)2, kan bruges som indikater for co2
Når Calciumhydroxid reagere med kuldioxid, vil der dannes et hvidt uopløseligt brundfald.
Volumenprocent eller vægtprocent
Volume= Rumfang
Vægtprocent= hvor meget det vejer
Ethanols massefylde(cirka) = 0,8 g/ml
500ml Ethanol vejer 400g
500ml vand vejer 500g
En overraskelse
Burde give: 500ml vand + 500ml ethanol =1000ml
Men giver i virkeligheden: 500ml vand + 500ml ethanol = 960ml
500ml vand blandet ed 500ml ethanol giver altså
En vægt på 900g og en volumen på 960ml.
Hvor mange procent udgør 400g af 900g?
400/900*100=44,44%
Hvor mange procent udgør 500ml af 960ml?
500/960*100=52,08%
Når man ser på en flaske spiritus er det angivet i volumen fordi det er den højeste procent.
Gæring og destillation
Ethanol dannes ved en kemisk proces, når glukose (druesukker), c6h1206 under oxygenfrie forhold er i kontakt med bagegær. Samtidig dannes culdioxid, der er en gas. Når gærbrød hæver, skyldes det netop carbondioxid, dannes ved gæring af sukker. Reaktionsskemaet ser sådan ud:
C2H12O6à2C2H5OH+2CO2
Gæringsprocessen foregår bedst under lun temperatur og når gæret får produceret nok ethanol ca. 12-14 % vil gæren dræbe sig selv.
Ved destillationen udnytter vi det ved at ethanol og vand har forskellige kogepunkt, og derved kun opvarme så ethanolen fordamper. Derved kan vi producere næsten ren ethanol. Vores destillat nåede en alkoholprocent på ca. 55%. Man vil aldrig kunne producere 100% ren ethanol, der vil altid være lidt vand bundet til alkoholen, derfor er det fineste man kan opnå ca. 96-98% ren ethanol.
Ethanol til ethanal:
2CH3CH2OH+O2 (cu)à 2CH3CHO+2H2O
(Ethanol) (Ethanal)
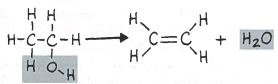
Ethanol til ethen:
C2H5OH à C2H4+H2O
Formlen for Ethanol er C2H5OH
Når endelsen er OH i den kemiske benævnelse så er det et alkohol.
Molekyler, hvor der indgår carbonatomer defineres som organiske forbindelser. Der er dog 2 undtagelser CO2 og CO, fordi de er uorganiske.
· Ethanol er en farveløs væske,
· Kogepunkt=78 grader,
· Frysepunkt=-117 grader
· Massefylden= 0,795 g/ml
Når ethanol brænder forekommer en fuldstændig forbrænding.
Afstemmes:
CO2H5OH+3Oà2CO2+3H20
Vand og kuldioxid kan ikke brænde derfor defineres det som en fuldstændig forbrænding.
Ånding er også en fuldstændig forbrænding (der dannes vand og kuldioxid)
Ånding er: Respiration og fotosyntese.
Kalkvand-Ca(OH)2, kan bruges som indikater for co2
Når Calciumhydroxid reagere med kuldioxid, vil der dannes et hvidt uopløseligt brundfald.
Volumenprocent eller vægtprocent
Volume= Rumfang
Vægtprocent= hvor meget det vejer
Ethanols massefylde(cirka) = 0,8 g/ml
500ml Ethanol vejer 400g
500ml vand vejer 500g
En overraskelse
Burde give: 500ml vand + 500ml ethanol =1000ml
Men giver i virkeligheden: 500ml vand + 500ml ethanol = 960ml
500ml vand blandet ed 500ml ethanol giver altså
En vægt på 900g og en volumen på 960ml.
Hvor mange procent udgør 400g af 900g?
400/900*100=44,44%
Hvor mange procent udgør 500ml af 960ml?
500/960*100=52,08%
Når man ser på en flaske spiritus er det angivet i volumen fordi det er den højeste procent.
Gæring og destillation
Ethanol dannes ved en kemisk proces, når glukose (druesukker), c6h1206 under oxygenfrie forhold er i kontakt med bagegær. Samtidig dannes culdioxid, der er en gas. Når gærbrød hæver, skyldes det netop carbondioxid, dannes ved gæring af sukker. Reaktionsskemaet ser sådan ud:
C2H12O6à2C2H5OH+2CO2
Gæringsprocessen foregår bedst under lun temperatur og når gæret får produceret nok ethanol ca. 12-14 % vil gæren dræbe sig selv.
Ved destillationen udnytter vi det ved at ethanol og vand har forskellige kogepunkt, og derved kun opvarme så ethanolen fordamper. Derved kan vi producere næsten ren ethanol. Vores destillat nåede en alkoholprocent på ca. 55%. Man vil aldrig kunne producere 100% ren ethanol, der vil altid være lidt vand bundet til alkoholen, derfor er det fineste man kan opnå ca. 96-98% ren ethanol.
Ethanol til ethanal:
2CH3CH2OH+O2 (cu)à 2CH3CHO+2H2O
(Ethanol) (Ethanal)
Ethanol til ethen:
C2H5OH à C2H4+H2O
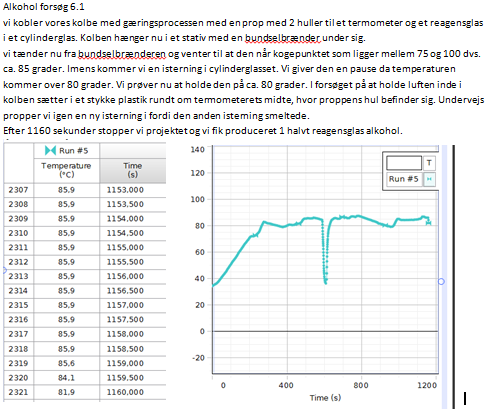
Alkohol forsøg fra bogen
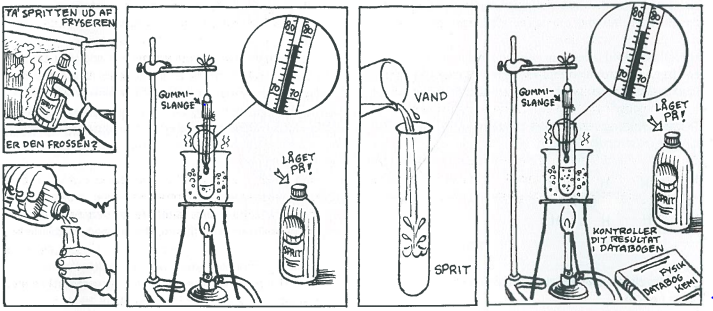
Vi har i dette forsøg sat et bægerglas med vand på et stativ over en bundselbrænder. I dette bægerglas har vi sænket et reagensglas med 4-5 ml sprit, som hænger på et stativ, så at sprittens overflade rammer vandets overflade. Vi har derudover koblet en temperaturmåler til computeren, og denne temperaturmåler har vi sænket ned i reagensglasset med sprit præcist sådan at den ikke rører spritten eller reagensglassets kant, fordi at vi kun skal måle dampens temperatur.
Vi tænder bundselbrænderen og ser temperaturen stige. Vores temperatur steg efter 200 sekunder op på 54 grader da at vores bægerglas begyndte at revne, hvilket fik os til at stoppe forsøget. Vi forsøger igen, hvor at bægerglasset ikke revner og temperaturen stopper med at stige ved 74,5 grader celsius.
Vi har fundet ud af at temperaturen stoppede med at stige, fordi at spritten havde nået sit kogepunkt, og vi har derudover fundet ud af at sprittens kogepunkt er mindre end vandets kogepunkt, da at spritten begyndte at koge før vandet.
Vi tænder bundselbrænderen og ser temperaturen stige. Vores temperatur steg efter 200 sekunder op på 54 grader da at vores bægerglas begyndte at revne, hvilket fik os til at stoppe forsøget. Vi forsøger igen, hvor at bægerglasset ikke revner og temperaturen stopper med at stige ved 74,5 grader celsius.
Vi har fundet ud af at temperaturen stoppede med at stige, fordi at spritten havde nået sit kogepunkt, og vi har derudover fundet ud af at sprittens kogepunkt er mindre end vandets kogepunkt, da at spritten begyndte at koge før vandet.
Alkohol Forsøg 3.1
Alkohol Forsøg 3.1
Vi tager en lighter og en ske og i rækkefølge fylder den med en blanding af vand og en bestemt procent ethanol. I forsøget starter vi med at tænde lighteren over væsken og bagefter under væsken.
Ethanol blanding med 20%:
Væsken brænder ikke, da at vi tænder den uden at varme den op først.
Da at vi senere hen varmede den op kunne vi heller ikke få ild i den
Ethanol blanding med 40%:
Væsken brænder ikke, da at vi tænder den uden at varme den op først.
Da at vi senere hen varmede den op kunne vi godt få ild i den
Ethanol blanding med 60%:
Væsken begynder allerede at brænde da at vi tænder den uden at varme den op først.
Da at vi senere hen varmede den op kunne vi sagtens også godt få ild i den.
Konklusion.
Vi har nået frem til at væsken brænder nemmere jo flere procent ethanol der er i blandingen.
Vi tager en lighter og en ske og i rækkefølge fylder den med en blanding af vand og en bestemt procent ethanol. I forsøget starter vi med at tænde lighteren over væsken og bagefter under væsken.
Ethanol blanding med 20%:
Væsken brænder ikke, da at vi tænder den uden at varme den op først.
Da at vi senere hen varmede den op kunne vi heller ikke få ild i den
Ethanol blanding med 40%:
Væsken brænder ikke, da at vi tænder den uden at varme den op først.
Da at vi senere hen varmede den op kunne vi godt få ild i den
Ethanol blanding med 60%:
Væsken begynder allerede at brænde da at vi tænder den uden at varme den op først.
Da at vi senere hen varmede den op kunne vi sagtens også godt få ild i den.
Konklusion.
Vi har nået frem til at væsken brænder nemmere jo flere procent ethanol der er i blandingen.
Forsøg 3.3
Vi tager et tørt syltetøjsglas hvori vi har taget en prop på. I en påselænskål har vi puttet en klump glasuld i hvorpå vi har hældt 3ml sprit på. Vi har også hældt 10ml kalkvand i et glas som vi skal bruge senere.
Vi starter med at sætte ild til glasuldet med sprit med en lang pind af træ, som brænder i enden, så ulden og spritten bliver tændt med vores hænder i en sikker afstand. Da der er ild i glasuldet, vender vi syltetøjsglasset omvendt og holder det over glasuldet, så at glasset bliver fyldt med den gas glasulden udleder når den bliver brændt. Når at glasset er fyldt med gas hælder vi kalkvand i, tager proppen på og ryster glasset. Vi kan nu se at glasset er blevet helt grumset. Derefter hældte vi en co2 indikator i form af en rød væske i, som blev gul da den kom i glasset. Denne gule farve beviser at der er co2 i glasset hvilket betyder at processen i forbrænding af sprit udgiver co2.
vi tager nu et andet tørt syltetøjsglas, som vi denne gang blot ånder i hvorefter vi igen vil tage proppen på, ryste den godt og grundig, tage vi proppen af og denne gang hælde vandfrit kobbersulfat i. Da vi ikke har noget vandfrit, varmer vi ikke vandfrit kobbersulfat op til det bliver gråt. Da vi hælder kobbersulfatet i syltetøjsglasset bliver selve kobbersulfatet blåt. Den blå farve beviser at der er vand i glasset, hvilket betyder at vores ånde indeholder vand.
Vi starter med at sætte ild til glasuldet med sprit med en lang pind af træ, som brænder i enden, så ulden og spritten bliver tændt med vores hænder i en sikker afstand. Da der er ild i glasuldet, vender vi syltetøjsglasset omvendt og holder det over glasuldet, så at glasset bliver fyldt med den gas glasulden udleder når den bliver brændt. Når at glasset er fyldt med gas hælder vi kalkvand i, tager proppen på og ryster glasset. Vi kan nu se at glasset er blevet helt grumset. Derefter hældte vi en co2 indikator i form af en rød væske i, som blev gul da den kom i glasset. Denne gule farve beviser at der er co2 i glasset hvilket betyder at processen i forbrænding af sprit udgiver co2.
vi tager nu et andet tørt syltetøjsglas, som vi denne gang blot ånder i hvorefter vi igen vil tage proppen på, ryste den godt og grundig, tage vi proppen af og denne gang hælde vandfrit kobbersulfat i. Da vi ikke har noget vandfrit, varmer vi ikke vandfrit kobbersulfat op til det bliver gråt. Da vi hælder kobbersulfatet i syltetøjsglasset bliver selve kobbersulfatet blåt. Den blå farve beviser at der er vand i glasset, hvilket betyder at vores ånde indeholder vand.
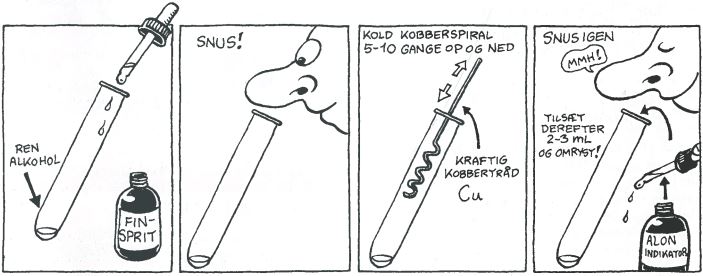
Forsøg 5.1
Vi har puttet ren alkohol i et reagensglas og lugtet til det uden at opfange en lugt. Senere ryster vi til det og kan nu lugte spritten. Vi dypper en spiralformet kobbertråd i reagensglasset. Den ændrer ikke lugten, men gør dog lugten stærkere og mere intens. Vi kommer alon indikator i og vi opdager nu, at der kommer bundfald.
Nu tager vi et nyt reagensglas, som vi også fylder med lidt sprit. Vi varmer nu kobbertråden op med en bundselbrænder. Vi stikker den varme kobbertråd i sprittet og det begynder at lugte mærkeligt.
Nu tager vi et nyt reagensglas, som vi også fylder med lidt sprit. Vi varmer nu kobbertråden op med en bundselbrænder. Vi stikker den varme kobbertråd i sprittet og det begynder at lugte mærkeligt.
Gæring
25g sukker
vand
gær (behøves ikke at blive vejet)
ingen gæringssalt
brug kun tegning 1 og 3
Vi tager en koble og hælder 25g sukker i, som omrystes indtil det bliver opløst. Vi hælder derefter 200 ml vand deri samt 10 g gær, som også opløses. Senere sætter vi en prop med et hul på, som vi putter et glasrør i hullet og kobler glasrøret til en slange. Slangen sættes til et andet glasrør, som sættes i en anden prop i et reagensglas med fyldt med ¼ vand.
Meningen med projektet er at lave en gæring hvor der opstår alkohol og Co2. Grunden til at gæren producere alkohol er at den ikke får luft. I forhold til når man bager.
vand
gær (behøves ikke at blive vejet)
ingen gæringssalt
brug kun tegning 1 og 3
Vi tager en koble og hælder 25g sukker i, som omrystes indtil det bliver opløst. Vi hælder derefter 200 ml vand deri samt 10 g gær, som også opløses. Senere sætter vi en prop med et hul på, som vi putter et glasrør i hullet og kobler glasrøret til en slange. Slangen sættes til et andet glasrør, som sættes i en anden prop i et reagensglas med fyldt med ¼ vand.
Meningen med projektet er at lave en gæring hvor der opstår alkohol og Co2. Grunden til at gæren producere alkohol er at den ikke får luft. I forhold til når man bager.
Forsøg 12.1
Opstilling:
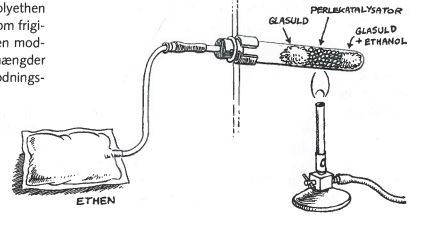
I dette forsøg startede vi med at tage en bunsenbrænder, et stativ, et reagensglas, en prop med et hul, et glasrør (så kort som muligt + helst lige, en slange (så kort, som muligt) og en hospitals-blodpose med mundstykke. I reagensglasset kom vi først et lag af glasuld og ethanol præcist så alt ethanolet vil blive absorberet. Derefter et lag på 4-5cm af perlekatalysatorer og til sidst endnu et lag af glasuld, men denne gang uden ethanol. Vi drypper ethanolen i med en pipette og trykker glasuldet ned med en spatel.
Vi sætter proppen på reagensglasset, kobler proppenshul til hospitalsposen via et glasrør og en slange. Vi stiller reagensglasset på stativet og placere det over en bunsenbrænder.
I dette forsøg startede vi med at tage en bunsenbrænder, et stativ, et reagensglas, en prop med et hul, et glasrør (så kort som muligt + helst lige, en slange (så kort, som muligt) og en hospitals-blodpose med mundstykke. I reagensglasset kom vi først et lag af glasuld og ethanol præcist så alt ethanolet vil blive absorberet. Derefter et lag på 4-5cm af perlekatalysatorer og til sidst endnu et lag af glasuld, men denne gang uden ethanol. Vi drypper ethanolen i med en pipette og trykker glasuldet ned med en spatel.
Vi sætter proppen på reagensglasset, kobler proppenshul til hospitalsposen via et glasrør og en slange. Vi stiller reagensglasset på stativet og placere det over en bunsenbrænder.
Forsøget:
Vi tænder bunsenbrænderen, og fokusere på at få flammen til kun at ramme perlekatalysatorerne. Efter kort til kan vi se, at der bliver udledt meget røg fra glasuldet. Dette røg bliver sendt ud til hospitalsposen og fylder den op med røgen. Man kan se at reagensglasset bliver rødglødende. Posen begynder at blive fyldt op med luft, og også en væske. Når der er kommet nok luft i posen slukker vi for bunsenbrænderen.
Konklusion:
Vi har nu lavet forsøget, og dette er hvad vi er kommet frem til der skete inde i reagensglasset. Ved hjælp af katalysatoren omdannede vi ethanolen til ethen og vand. Derfor blev urinposen fyldt med dels væsken, som var ethen, og røgen, som var damp, dvs. opvarmet vand.
Vi tænder bunsenbrænderen, og fokusere på at få flammen til kun at ramme perlekatalysatorerne. Efter kort til kan vi se, at der bliver udledt meget røg fra glasuldet. Dette røg bliver sendt ud til hospitalsposen og fylder den op med røgen. Man kan se at reagensglasset bliver rødglødende. Posen begynder at blive fyldt op med luft, og også en væske. Når der er kommet nok luft i posen slukker vi for bunsenbrænderen.
Konklusion:
Vi har nu lavet forsøget, og dette er hvad vi er kommet frem til der skete inde i reagensglasset. Ved hjælp af katalysatoren omdannede vi ethanolen til ethen og vand. Derfor blev urinposen fyldt med dels væsken, som var ethen, og røgen, som var damp, dvs. opvarmet vand.