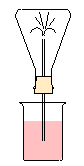Kemisk produktion - arbejdsark 1
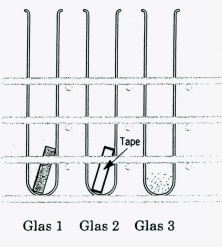
Vi har tre reagensglas, den 1. har en lille plade af zink, den anden har også en plade af zink, dog med tape omkring, og en med zinkpulver. Vi fylder alle tre reagensglas 1/3 op med syre, og ser nu hvilket reagensglas der først bliver ”zink-fri”, og det ser ud til at det er zinkpulveret der er hurtigst, zinkpladen der er anden-hurtigst og zinkpladen med tape der er langsomst. Det foregår i denne rækkefølge fordi at jo større overlag af zink syren har adgang til jo hurtigere går processen med omdannelsen. Ved rent pulver har syren adgang til det hele, derfor går det hurtigst at omdanne, ved zinkpladen har syren adgang til overfladen og bunden mens ved zinkpladen med tapen dækker tapen for den ene overflade så derfor er zinkpladen uden tape før den med tape.
Kemisk produktion - arbejdsark 2
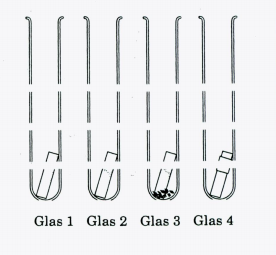
I Dette forsøg skulle vi gøre det nogenlunde samme bare med 4 reagensglas og andet fyld i dem. I det 1. glas havde vi et blank zinkstykke, som ikke var brugt før, i det 2. glas havde vi et lille stykke kobberfolie, som er slebet blankt med ståluld, i det 3. glas have vi lidt kobberspåner medet og et blankt zinkstykke ovenpå og til sidst i det 4. glas havde vi et blankt stykke zink med et sykke kobber viklet rundt om.
Da vi havde hældt tingene op skulle vi hælde syre oveni og se hvad der blev omdannet hurtigst. Den hurtigste var glas nr. 3, derefter glas nr. 1, derefter glas nr. 4 og den langsommeste var glas nr. 2. Forsøget viste, at reaktonshastigheden er størst hvor kobberet er i tættest kontakt med zinken.
Da vi havde hældt tingene op skulle vi hælde syre oveni og se hvad der blev omdannet hurtigst. Den hurtigste var glas nr. 3, derefter glas nr. 1, derefter glas nr. 4 og den langsommeste var glas nr. 2. Forsøget viste, at reaktonshastigheden er størst hvor kobberet er i tættest kontakt med zinken.
kemisk produktion - arbejdsark 3-4
vi har hældt 2 tsk. fulde kobbersulffat i et bægerglas med ca. 100 ml. vand pg har røret godt rundt og filtreret det. derefter ville vi holde zinken i det filtrerede væske i 30 sekunder. Da at vi derefter tog zinken op og tørede det opdagede vi at stykkets overlag var helt sort. Vi tog derefter zinkstykket og puttede det i normal svovlsyre. Reaktionen på dette var, at det blev omdannet til hydrogen, der bobler op på overfladen. Derefter høldte vi lidt af den filtrerede væske oveni og holdte et glas overfor mens vi tændteen ligter og holdt den over da vi fjernede glasset, der resulterede en lille gaseksplosion.
Kemisk produktion - arbejdsark 5-7
Vi har blandet de 2 stoffer kaldt selmiak og melkalk i et reagensglas på et stativ. Derefter blandede vi dem sammen med en spatel og de begyndte at lugte :(
Derefter tog vi et bægerglas med 5-10 dråber fanolftalein og 250 ml parafinolie.derefter tænder vi en bundselbrænder under reagensglasset og rører samtidig rundt med en spatel. Vi holder et andet reagensglas over det første for at opsuge den røg der siver op. Derefter sætter vi det ned i bægerglasset hvor der sker en kemisk reaktion. Væsken bliver lilla og stiger langsom op ad reagensglasset. Den fik farve fordi phenolphalin er en farveindikator, dog er det denne farve fordi det er en base.
Vi prøvede det derefter igen med et endnu større glas, og puttede en prop med hul og lille glasrør igennem for at få en endnu større virkning.
2Ng,Cl + Ca(OH)2 -> 2 NH3 + CaCl2 + 2 H2O
Derefter tog vi et bægerglas med 5-10 dråber fanolftalein og 250 ml parafinolie.derefter tænder vi en bundselbrænder under reagensglasset og rører samtidig rundt med en spatel. Vi holder et andet reagensglas over det første for at opsuge den røg der siver op. Derefter sætter vi det ned i bægerglasset hvor der sker en kemisk reaktion. Væsken bliver lilla og stiger langsom op ad reagensglasset. Den fik farve fordi phenolphalin er en farveindikator, dog er det denne farve fordi det er en base.
Vi prøvede det derefter igen med et endnu større glas, og puttede en prop med hul og lille glasrør igennem for at få en endnu større virkning.
2Ng,Cl + Ca(OH)2 -> 2 NH3 + CaCl2 + 2 H2O
Ethanol til ethanal : katalyse
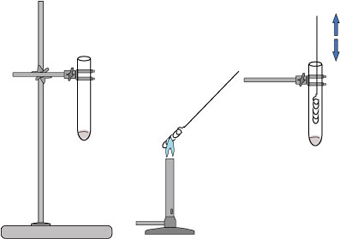
I dette forsøg tog vi et reagensglas og tilførte 10 dråber sprit, og gled det ud på kanterne. Derefter skulle vi tage en spiralformet kobbertråd som vi førte op og ned af reagensglasset, dog uden at røre spritten eller kanten. Dette fik ingen virkning på reagensglassets lugt af sprit eller kobbertrådens farve. Derefter prøvede vi at sætte kobbertråden over en bundselbrænder. da at den er helt rødglødende føre vi den igen op og ned gennem reagensglasset, og dette gjorde kobbertråden helt hvid, og fik spritten og reagensglasset til istedet for sprit at lugte lidt af krudt.
N2 - fremstilling i laboratoriet til brug ved NH3 - syntese
I dette forsøg skulle vi finde en rør med to ender og proppe stål uld i midten, og derefter sætte to propper med hul i hver ende og sætte to oppustede urinposer i hullerne. Derefter tog vi en bundselbrænder under røret. Da vi har slukket bundselbrænderen klemte vi på urinposerne og stålulden begyndte at lyse rødt, dvs gløde. Vi gjorde det igen, men denne gang begyndte stålulden ikke at gløde. Dette sker fordi at alt ilten inde i røret og urinposerne er væk, omdannet til N2 (kvælstof). Luften inde i røret er helt iltfrit og derfor kan ild eller gløder ikke opstå.
Fysik forsøg om paraffinolie
Vi skulle i dette forsøg have en bundeslbrænder. Over den skulle der være et reagensglas på et stativ. Reagensglasset har en prop med et hul, som med en slange får connecter til et andet reagensglas med en prop med to huller. Reagensglassets andet hul bliver forbundet til en urionpose. I det første reagensglas over bundselbrænderen blev fyldt med; først 2 centimeters glasuld, hvor der er blevet dryppet parrafinolie, indtil overlaget er blevet vådt. Derefter kommer perleskatalysatorer i, ca. omkring 2-3 cm. Til sidst kom der igen lige et tyndt overlag af glasuld. Vi begyndte derefter at tænde bundselbrænderen, lige under perlerne. Dette blev vi ved med indtil at urinposen blev halvt fyldt med gas. Undervejs kom en brunlig væske også kaldt benzin ind i det andet reagensglas, og det første reagensglas begyndte at blive fyldt med røg. Derefter tog vi Urinposen med røgen, og væsken i det andet bægerglas og satte ild til det. Det var yderst brændbart. Dette skete fordi at parrafinoliemolekylerne bliver under temperaturen delt i flere stoffer; nonan, brutan, propan, ethen og kulstof. Stoffet nonan er den brune væske, dvs benzinen. Det der var med til at give farven til det var dog ethen. Brutan og propan var derimod de gasser der opstod i den kemiske proces og kom ind i urinposen.
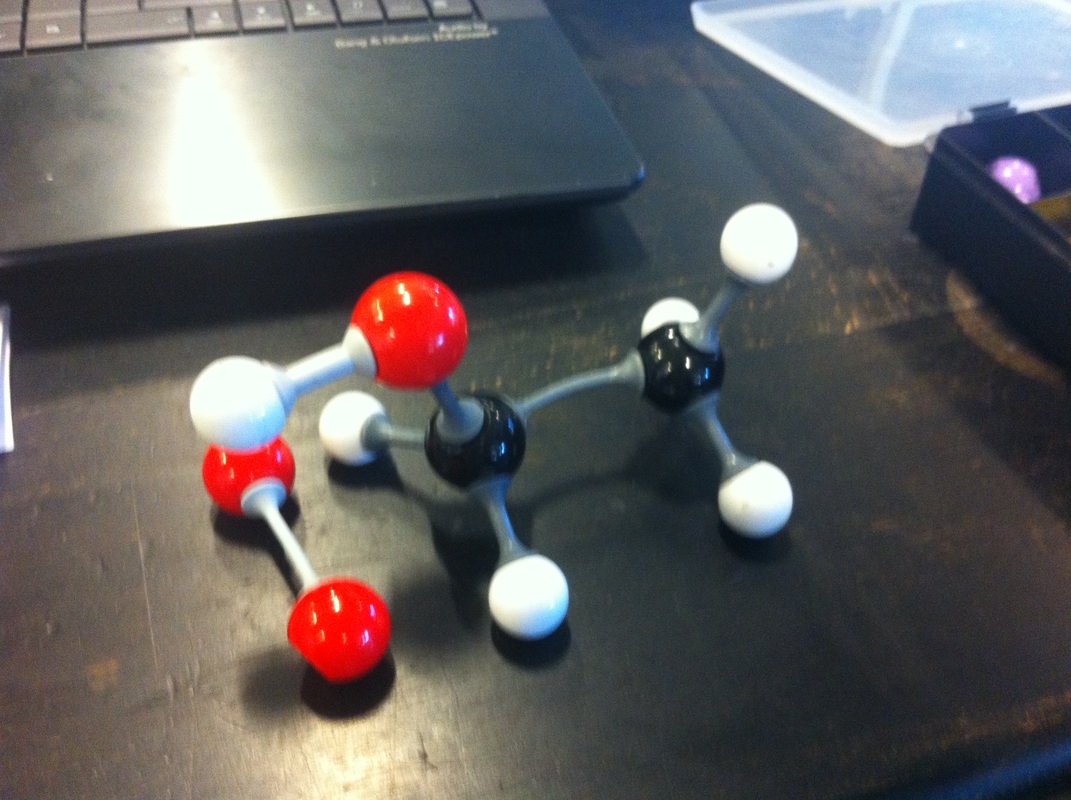
Molekyler i de forskellige forsøg
Ethanol til ethen (side 18)
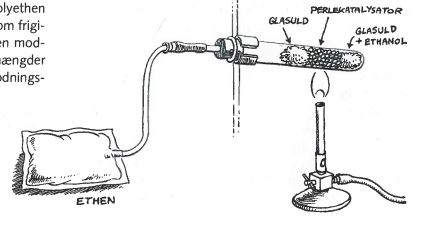
Opstilling:
I dette forsøg startede vi med at tage en bunsenbrænder, et stativ, et reagensglas, en prop med et hul, et glasrør (så kort som muligt + helst lige, en slange (så kort, som muligt) og en hospitals-blodpose med mundstykke. I reagensglasset kom vi først et lag af glasuld og ethanol præcist så alt ethanolet vil blive absorberet. Derefter et lag på 4-5cm af perlekatalysatorer og til sidst endnu et lag af glasuld, men denne gang uden ethanol. Vi drypper ethanolen i med en pipette og trykker glasuldet ned med en spatel.
Vi sætter proppen på reagensglasset, kobler proppenshul til hospitalsposen via et glasrør og en slange. Vi stiller reagensglasset på stativet og placere det over en bunsenbrænder.
I dette forsøg startede vi med at tage en bunsenbrænder, et stativ, et reagensglas, en prop med et hul, et glasrør (så kort som muligt + helst lige, en slange (så kort, som muligt) og en hospitals-blodpose med mundstykke. I reagensglasset kom vi først et lag af glasuld og ethanol præcist så alt ethanolet vil blive absorberet. Derefter et lag på 4-5cm af perlekatalysatorer og til sidst endnu et lag af glasuld, men denne gang uden ethanol. Vi drypper ethanolen i med en pipette og trykker glasuldet ned med en spatel.
Vi sætter proppen på reagensglasset, kobler proppenshul til hospitalsposen via et glasrør og en slange. Vi stiller reagensglasset på stativet og placere det over en bunsenbrænder.
Forsøget:
Vi tænder bunsenbrænderen, og fokusere på at få flammen til kun at ramme perlekatalysatorerne. Efter kort til kan vi se, at der bliver udledt meget røg fra glasuldet. Dette røg bliver sendt ud til hospitalsposen og fylder den op med røgen. Man kan se at reagensglasset bliver rødglødende. Posen begynder at blive fyldt op med luft, og også en væske. Når der er kommet nok luft i posen slukker vi for bunsenbrænderen.
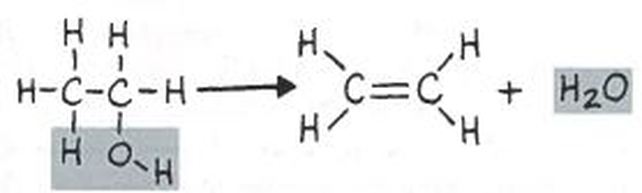
Konklusion:
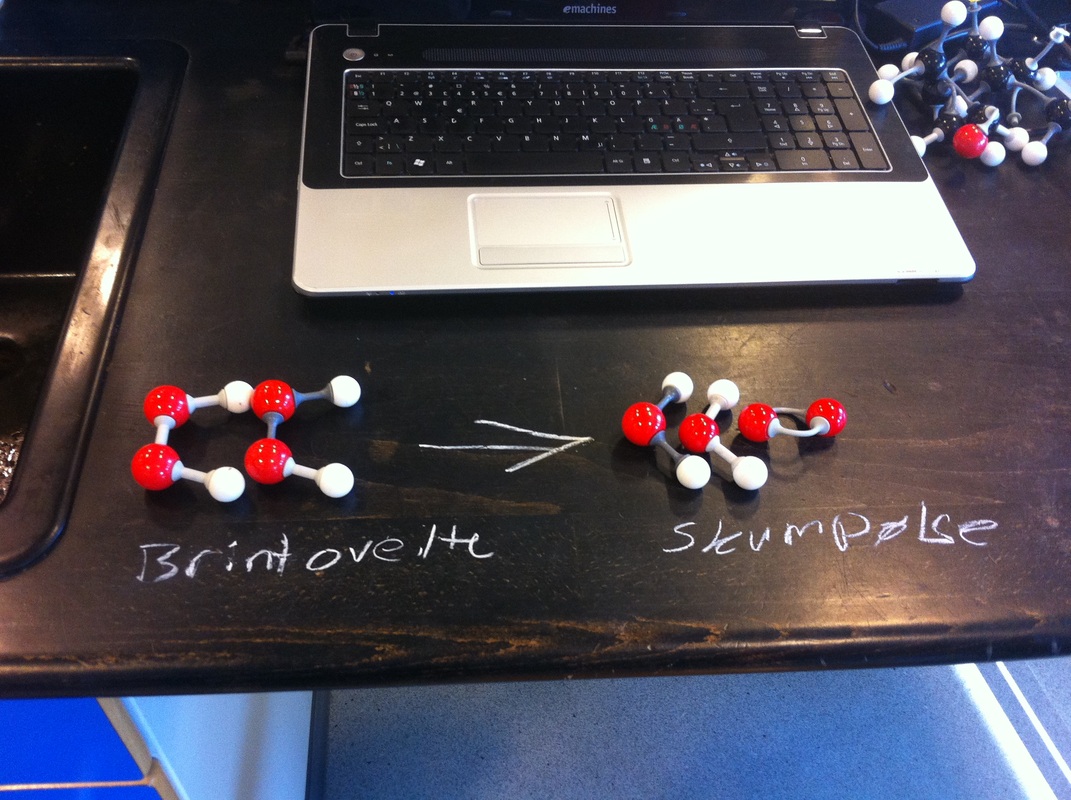
Vi har nu lavet forsøget, og dette er hvad vi er kommet frem til der skete inde i reagensglasset. Ved hjælp af katalysatoren omdannede vi ethanolen til ethen og vand. Derfor blev urinposen fyldt med dels væsken, som var ethen, og røgen, som var damp, dvs. opvarmet vand.
Vi tænder bunsenbrænderen, og fokusere på at få flammen til kun at ramme perlekatalysatorerne. Efter kort til kan vi se, at der bliver udledt meget røg fra glasuldet. Dette røg bliver sendt ud til hospitalsposen og fylder den op med røgen. Man kan se at reagensglasset bliver rødglødende. Posen begynder at blive fyldt op med luft, og også en væske. Når der er kommet nok luft i posen slukker vi for bunsenbrænderen.
Konklusion:
Vi har nu lavet forsøget, og dette er hvad vi er kommet frem til der skete inde i reagensglasset. Ved hjælp af katalysatoren omdannede vi ethanolen til ethen og vand. Derfor blev urinposen fyldt med dels væsken, som var ethen, og røgen, som var damp, dvs. opvarmet vand.