saccharid: sukker
Dissaccharid: to sammensatte sukkermolekyler
C12H22O11
monosaccharid: et sukkermolekyle
C6H12O5
Dissaccharid: to sammensatte sukkermolekyler
C12H22O11
monosaccharid: et sukkermolekyle
C6H12O5
Benedictsreagens
Vi fylder tre reagensglas op, som hver især er nummererede med numrene fra 1-3. Vi fylder reagensglasset med nummeret 1 med kartoffelmel, 2 med sukker og 3 med druesukker. Vi sørger for at der er lige meget i hvert reagensglas. Derefter fylder vi reagensglassene halvt op med vand og tilføre de 5 dråber lostle hvorefter vi ryster og blander væskerne sammen. Reagensglasset er blevet blev blåt. Vi skaffer en bundsel-brænder, stiller en trefod over den. Denne trefod tager vi et bægerglas, med vand i, oven på. Vi sætter derefter reagensglassene i bægerglasset og tænder for bundsel-brænderen. Efter et stykke tid er reagensglas 3 blevet grønt, derefter gult, derefter orange, og derefter brunt. Imens er reagensglas 1 blot blevet lidt lysere i bunden, og senere lidt grønt og reagensglas 2 har ikke fået en synlig betydelig ændring af farven. Reagensglassenes forskellige procestempoer har noget at gøre med sukkerindholdets opløsningstider. Da at kartoffelmelet og sukkeret består af disaccharid skulle man i processen skille de to sukkermolekyler, mens at druesukker består af monosaccharid og dermed i forvejen kun bestod af enkelte adskilte sukkermolekyler.
forsøg 7.1
Vi tager en bundsel-brænder og en trefod, hvorpå vi stiller et 250 ml bægerglas fyldt med 80 ml vand og tilsat ca. 1 g. sukker, hvorefter vi har rørt rundt indtil det var opløst. Derefter tilføjede vi 10 ml. fortyndet eddike syre. Vi tænder for bundselbrænderen og venter på at det koger. Derefter lader vi væsken koge i 5 min. når der er gået 5 minutter slukker vi bundsel-brænderen og lader det afkøle. Efter det er afkølet tager vi en spatel og hælder lidt af opløsningen på et indikatorpapir. Da at vi dryppede det på kom der en rødlig farve frem på papiret. Derefter tilføjer vi lidt ammoniak og røre rundt for at se om vi kan få den ønskede stabiliserede og neutrale væske og tester derefter farven på et andet stykke indikatorpapir. I vores andet forsøg blev væsken gul, og efter tredje forsøg gik det lige efter hensigten, da at farven på indikatorpapiret blev, efter tilføjelsen af ammoniak, farven grøn. Hvilket var farven, som viste stabiliseringen af væsken.
2 monosaccharider: glucose og fructose.
Til prøven: behøver ikke ændre farven til grøn, men bare vise spaltningen med ændringen af farven fra blå til rød/brun.
Det der sker er at eddikke-syren lige som vores mavesyre skiller dissacchariderne til monosaccharider.
2 monosaccharider: glucose og fructose.
Til prøven: behøver ikke ændre farven til grøn, men bare vise spaltningen med ændringen af farven fra blå til rød/brun.
Det der sker er at eddikke-syren lige som vores mavesyre skiller dissacchariderne til monosaccharider.
Bendedictreagens (2)
I dette forsøg vil vi gerne gøre det samme som i forsøget 7.1, men bare med flere forskellige sukkerarter, for at se forskellen.
I druesukkeret vælger vi ikke at putte eddikkesyrer i da at druesukkeret allerede er et monosaccharid.
Derefter bruger vi de samme væsker til forsøget benedictsreagens, og gør dette med den samme metode og dette blev vores resultater:
Sukker (dissacharid):I starten da vi kom lostle i blev det blåt (forventet). Da at processen var ovre var væskens farve uændret.
Druesukker (monosacharid) :I starten da vi kom lostle i blev det blåt (forventet).Da at processen var ovre var væskens farve ændret til en rødbrunlig farve.
Druesukkeret havde ændret farven i modsætning til det normale sukker, og dette er forventet, da at det er nemmere at opløse monosaccharider end dissacharider, da at dissachariderne i processen også skal skilles ad. Jo flere monosaccharider der er i blandingen, jo hurtigere og kraftigere farve var der
I druesukkeret vælger vi ikke at putte eddikkesyrer i da at druesukkeret allerede er et monosaccharid.
Derefter bruger vi de samme væsker til forsøget benedictsreagens, og gør dette med den samme metode og dette blev vores resultater:
Sukker (dissacharid):I starten da vi kom lostle i blev det blåt (forventet). Da at processen var ovre var væskens farve uændret.
Druesukker (monosacharid) :I starten da vi kom lostle i blev det blåt (forventet).Da at processen var ovre var væskens farve ændret til en rødbrunlig farve.
Druesukkeret havde ændret farven i modsætning til det normale sukker, og dette er forventet, da at det er nemmere at opløse monosaccharider end dissacharider, da at dissachariderne i processen også skal skilles ad. Jo flere monosaccharider der er i blandingen, jo hurtigere og kraftigere farve var der
Forsøg 7.2
I dette forsøg har vi taget 2 kartofler og skrabet dem med en smørrekniv hvorefter vi har skæret disse skrabede kartofler i små tern med den samme smørrekniv. Imens vi gjorde dette har vi fundet forskellige ting frem: 5 reagensglas, en spatel, en trefod under en bundselbrænder, to bægerglas; 1 med 500 ml og en med 250 ml, og til sidst har vi sat en temperaturmåler til computeren.
Det 500 ml bægerglas har vi nu fyldt halvt op og kartoffelstykkerne har vi nu lagt på et viskestykke, som vi har foldet sammen til en pose. Denne pose dypper vi i dette bægerglas gentagende gange hvorefter vi hver gang vrider posen, så den væske posen har opsamlet ryger ned i bægerglasset igen. Væsken begynder efterhånden at blive mindre gennemsigtig og får en mere hvid farve. Efter vi har gjort dette gentagende gange lader vi bægerglasset stå og venter indtil at der er dannet bundfald. Når der er kommet bundfald prøver vi at hælde væsken ud af bægerglasset, mens vi beholder bundfaldet deri. Derefter fylder vi det andet reagensglas på 250 ml op med 50 ml vand og lader det stå på trefoden, mens vi tænder bundselbrænderen og venter på at det koger. Når det begynder at koge tager vi bundfaldet ned i det lille bægerglas, mens at vi røre rundt. Imens renser vi det store bægerglas og fylder det op med 250 ml vand. Efter vi har røret bundfaldet og vandet sammen stiller vi så det lille bægerglas i det store bægerglas og lader væsken i det lille bægerglas afkøle indtil den er 40 grader
Det 500 ml bægerglas har vi nu fyldt halvt op og kartoffelstykkerne har vi nu lagt på et viskestykke, som vi har foldet sammen til en pose. Denne pose dypper vi i dette bægerglas gentagende gange hvorefter vi hver gang vrider posen, så den væske posen har opsamlet ryger ned i bægerglasset igen. Væsken begynder efterhånden at blive mindre gennemsigtig og får en mere hvid farve. Efter vi har gjort dette gentagende gange lader vi bægerglasset stå og venter indtil at der er dannet bundfald. Når der er kommet bundfald prøver vi at hælde væsken ud af bægerglasset, mens vi beholder bundfaldet deri. Derefter fylder vi det andet reagensglas på 250 ml op med 50 ml vand og lader det stå på trefoden, mens vi tænder bundselbrænderen og venter på at det koger. Når det begynder at koge tager vi bundfaldet ned i det lille bægerglas, mens at vi røre rundt. Imens renser vi det store bægerglas og fylder det op med 250 ml vand. Efter vi har røret bundfaldet og vandet sammen stiller vi så det lille bægerglas i det store bægerglas og lader væsken i det lille bægerglas afkøle indtil den er 40 grader
Derefter tager vi et reagensglas og spytter ned i det, og fylder det derefter halvt op med spyt og rystet det til det er blandet sammen. Derefter hælder vi denne blanding ned i de andre 4 reagensglas så de får lige meget hver. Når vi har gjort det, tilsætter vi derudover 1 dråbe stivelsesreagens i hvert glas. Derefter fylder vi 10 ml af vores stivelse fra bægerglasset ned i reagensglassene, 1 af gangen med 3 minutters mellemrum. Da vi hælder stivelsen i det første reagensglas og rører rundt bliver væsken helt mørkeblå inden for få sekunder. Imens kan man se at de andre reagensglas uden stivelsen er blevet gullige. Da vi tager det andet reagensglas bliver det også helt mørkeblåt, men man kan dog se en forskel mellem de to reagensglas, da at det første reagensglas har fået en anelse lysere blå farve. Det sidste reagensglas blev dog meget lysere end de andre. Dette skyldes at vi puttede mindre stivelse i den, fordi vi var løbet tør. Med det kan man sige at farven afhhænger af hvor meget stivelse der er kommet i glassen. Det der skete var at spyttets enzymer nedbrød stivelsen. Så det afhænger af balancemængden af spyt og stivelse
Forsøg 7.3
I dette forsøg har vi stillet en bunsenbrænder under en trefod. På denne trefod har vi stillet et 250 ml bægerglas med et reagensglas indeni. I det reagensglas er der 1/4 pastoriseret æggehvide. Vi har et andet reagensglas med lige så meget æggehvide i på et reagensglas stativ. Vi tænder for bunsenbrænderen og venter på at æggehviden stivner. Når det sker tager vi temperaturen på den. temperaturen var ca. 72 grader da at æggehviden stivnede.
Vi skulle derefter besvare hvorfor at vandbadet gav en langsommere opvarmning af æggehviden. Vi fandt svaret at den opvarmes langsommere, fordi at der også bliver brugt energi på at opvarme vandet. Vi prøver forsøget igen, denne gang med det andet reagensglas, dog hælder vi æggehviden ned i bægerglasset når vandet "næsten" koger. Vi rører i æggehviden mens vi kommer det i og efter alt æggehviden er kommet i slukker vi for bunsenbrænderen.
Opløsningen i bægerglasset er meget hurtig, da at væsken bliver stivnet næsten lige så snart som den kom i. Den bliver helt hvid og vi skynder os at røre hurtigt for at der ikke kommer klumper i
Vi hælder nu 3 ml af opløsningen i et reagensglas og tilføre natriumhydrooxid, til at rumfanget er fordoblet. derefter kommer vi 3-4 dråber kobbersulfat i og rører rundt med spatlen. Farven i reagensglasset er lilla, og dette påviser æggehvidens protein.
Vi hælder nu 3 ml af opløsningen i et reagensglas og tilføre natriumhydrooxid, til at rumfanget er fordoblet. derefter kommer vi 3-4 dråber kobbersulfat i og rører rundt med spatlen. Farven i reagensglasset er lilla, og dette påviser æggehvidens protein.
Forsøg 7.4
I dette forsøg har vi taget 2 reagensglas med propper i på et reagensglas stativ, en spatel, et bægerglas og et filtrerpapir.
1. På filtrerpapiret har vi dryppet en dråbe madolie på og en dråbe vand ved siden af, og derefter lagt papiret på en radiator.
Efter nogle minutter kan man ikke længere se hvor madolien har været.
2. Derefter har vi nu taget et af reagensglassene og hældt 2 ml vand i og den dobbelte mængde madolie. Med proppen på har vi nu rystet dette reagensglas kraftigt. Derefter lod vi det stå i nogle minutter. Efter disse minutter kan man se at vandet er i bunden, mens madolien ligger på toppen. Dette sker fordi at olien har en mindre massefylde end vand.
3. vi Har hældt en halv tsk. magarine i et reagensglas og tilført 5 ml. sprit og rystet. Glasset er fyldt med en tyk klump fedt, og langsomt kan man se at den bliver mindre. Det der sker er at sprittten opløser fedtet. og fedtet står nu tilbage som nogle langsomt opløsende klumper i glasset.
4. Vi tager nu 5 ml vand oveni og rystet igen. Efter vi har ventet i nogle minutter kan vi nu konkludere, at opløsningen nu går langsommere. Dette gør den fordi at spritten nu er mindre koncentreret og dermed mindre kraftig.
1. På filtrerpapiret har vi dryppet en dråbe madolie på og en dråbe vand ved siden af, og derefter lagt papiret på en radiator.
Efter nogle minutter kan man ikke længere se hvor madolien har været.
2. Derefter har vi nu taget et af reagensglassene og hældt 2 ml vand i og den dobbelte mængde madolie. Med proppen på har vi nu rystet dette reagensglas kraftigt. Derefter lod vi det stå i nogle minutter. Efter disse minutter kan man se at vandet er i bunden, mens madolien ligger på toppen. Dette sker fordi at olien har en mindre massefylde end vand.
3. vi Har hældt en halv tsk. magarine i et reagensglas og tilført 5 ml. sprit og rystet. Glasset er fyldt med en tyk klump fedt, og langsomt kan man se at den bliver mindre. Det der sker er at sprittten opløser fedtet. og fedtet står nu tilbage som nogle langsomt opløsende klumper i glasset.
4. Vi tager nu 5 ml vand oveni og rystet igen. Efter vi har ventet i nogle minutter kan vi nu konkludere, at opløsningen nu går langsommere. Dette gør den fordi at spritten nu er mindre koncentreret og dermed mindre kraftig.
Forsøg 7.5
1. Rema 1000 flydende
2. tusindfryd magarine
3. Rema 1000 Magarine
4. plantemagarine.
VI tager 4 reagensglas og fylder dem hver med disse ovenstående produkter. Vi putter disse reagensglas i et bægerglas, som står oven på en trefod på en bunsenbrænder. Bægerglasset er på 90 grader, og vi vil prøve at holde den på den temperatur, I magarinerne har vi lavet et hul med en træpind, for at der kan komme luft op til alt magarinen og det ikke kun er bunden, som bliver varm.
1. Rema 1000 flydende:
0,3 cm vand
5 cm olie
5,3 cm i alt
vandindhold %: 6%
2. tusindfryd magarine:
1 cm vand
3 cm olie
4 cm i alt
vandindhold %: 33%
3. Rema 1000 Magarine:
0,75 cm vand,
3,5 cm olie,
4,25 cm i alt
vandindhold %: 21,4%
4. plantemagarine:
2 cm vand,
3,5 cm olie
5,5 cm i alt
vandindhold %: 57%
Vi fandt ud af at der var mest olie i flydende magarine, og mest vand i plantemagarine.
2. tusindfryd magarine
3. Rema 1000 Magarine
4. plantemagarine.
VI tager 4 reagensglas og fylder dem hver med disse ovenstående produkter. Vi putter disse reagensglas i et bægerglas, som står oven på en trefod på en bunsenbrænder. Bægerglasset er på 90 grader, og vi vil prøve at holde den på den temperatur, I magarinerne har vi lavet et hul med en træpind, for at der kan komme luft op til alt magarinen og det ikke kun er bunden, som bliver varm.
1. Rema 1000 flydende:
0,3 cm vand
5 cm olie
5,3 cm i alt
vandindhold %: 6%
2. tusindfryd magarine:
1 cm vand
3 cm olie
4 cm i alt
vandindhold %: 33%
3. Rema 1000 Magarine:
0,75 cm vand,
3,5 cm olie,
4,25 cm i alt
vandindhold %: 21,4%
4. plantemagarine:
2 cm vand,
3,5 cm olie
5,5 cm i alt
vandindhold %: 57%
Vi fandt ud af at der var mest olie i flydende magarine, og mest vand i plantemagarine.
forsøg 7.6
I dette forsøg skulle vi lave vores egen læskedrik og prøve at finde de bedste opskrifter. I starten skulle vi obligatorisk tage et 250 ml plastbæger og hældt 200 ml vand i, og derefter 3 tsk. sukker, 0,5 tsk cirtonsyre for at give drikken en smule smag. derefter kunne vi selv vælge om vi kunne tilsætte natron for brus og salt for at gøre den isotonisk, dvs den har det samme mængdeforhold mellem vand og salt, som i kroppens blodceller. Vi har valgt at tage 1 tsk. Salt i, samt 1 tsk. natron. For at gøre drikken spændende og fancy har vi valgt at tilføre blå farve. Vi syntes at den smagte meget saltet og syrlig, så vi valgte at tilsætte 1 tsk. Sukker, og senere 1 tsk sukker igen. Dette virkede ikke specielt på smagen, og vi tror at fejlen var at vi startede med at tage for meget salt, vi skulle have gået mere i dybden og tilpasset mængdeforholdet iforhold til væsken i kroppen.
Dette kan man bruge i hverdagen til at fremstille læskedrikke
Dette kan man bruge i hverdagen til at fremstille læskedrikke
Forsøg 7.7
I dette forsøg skulle vi bruge 2 bægerglas på 250 ml, en spatel, en bunsenbrænder og en trefod med keramisk trådnet, et termometer. og derudover bomuldslærred, husholdningseddike og skummetmælk.
Vi starter med at hælde 50 ml af skummetmælk og 10 ml af eddike i et af bægerglassene og rører det sammen med spatellen, og vi kan se at der i den hvide væske langsomt bliver dannet nogle hvide klumper. Vi prøver nu at hælde væsken i det andet bægerglas gennem et filtrerpapir. Man kan se at det eneste der kommer igennem filtrerpapiret og ned i bægerglasset er gennemsigtig væske. Da at alt væsken er kommet i, står filtrerpapiret tilbage kun med en tyk, klumpet og ikke flydende masse.
Vi skylder nu det første bægerglas for mælken og fylder det op med mælk og dypper nu filtrerposen med de klumpede rester. Hver gang vi har dyppet den en gang vrider vi den så at væsken løber fra. Når vi har gjort dette er der nu i det foldede filtrerpapir starten på en ost.
Vi tager nu det andet bægerglas med væsken fra før og sætter den op på bunsenbrænderen. Vi opvarmer nu væsken op til ca. 80 grader og ser at der langsomt bliver dannet en masse små hvide fnug. Vi hælder nu væsken over i det første bægerglas, som vi har gjort rent igen, gennem en tragt. Gennem traget kommmer der igen en mere gennemsigtig væsken. Denne væske, som vi i dette bægerglas har dannet er mælkesukker.
Vi starter med at hælde 50 ml af skummetmælk og 10 ml af eddike i et af bægerglassene og rører det sammen med spatellen, og vi kan se at der i den hvide væske langsomt bliver dannet nogle hvide klumper. Vi prøver nu at hælde væsken i det andet bægerglas gennem et filtrerpapir. Man kan se at det eneste der kommer igennem filtrerpapiret og ned i bægerglasset er gennemsigtig væske. Da at alt væsken er kommet i, står filtrerpapiret tilbage kun med en tyk, klumpet og ikke flydende masse.
Vi skylder nu det første bægerglas for mælken og fylder det op med mælk og dypper nu filtrerposen med de klumpede rester. Hver gang vi har dyppet den en gang vrider vi den så at væsken løber fra. Når vi har gjort dette er der nu i det foldede filtrerpapir starten på en ost.
Vi tager nu det andet bægerglas med væsken fra før og sætter den op på bunsenbrænderen. Vi opvarmer nu væsken op til ca. 80 grader og ser at der langsomt bliver dannet en masse små hvide fnug. Vi hælder nu væsken over i det første bægerglas, som vi har gjort rent igen, gennem en tragt. Gennem traget kommmer der igen en mere gennemsigtig væsken. Denne væske, som vi i dette bægerglas har dannet er mælkesukker.
forsøg 7.8
1. Vi skulle tage et bægerglas og fylde det op med en halv teskefuld citronsyre og tilføre lidt vand og derefter måle ph-værdien. ph-værdien viste negativ, da ph indikatoren viste en rød farve
2. Vi skulle tage vores andet bægerglas og fylde det op med en halv teske fuld natron og tilføre lidt vand. Derefter målte vi igen ph-værdien og ph-indikatoren viste en grøn farve, dvs at den var basis.
3. Vi har nu vasket glassene og tilført dem tre forskellige stoffer. den tilførte vi 1. citronsyger og sukker med vand. Dette bægerglas bobler en lillesmule. Den 2. bægerglas fyldte vi med natron og sukker. Dette bægerglas viser ingen kemisk reaktion. det 3. bægerglas fyldte vi med citronsyger og natron. Dette bægerglas boblede kraftigt.
4. Vi har taget et stort bægerglas og tilført dem citronsyre og natron uden vand. pulverne citronsyre og natron reagere ikke på hinanden
5. Vi tilføre det stor bægerglas med 50 ml vand og stofferne citronsyre og natron reagere nu kraftigt ved at boble.
Vi sætter nu ild til en træ-pind og prøver at sætte den ned i det store bægerglas. Den slukkede pludseligt da den nærmede sig væsken. Vi prøvede igen, og dette forsøg viste samme resultat. Røgen fra den slukkede træpind forbliver dog i bægerglasset.
Forklaring:
Røgen forbliver i glasset, fordi at den er tungere end luft, og derfor ikke kan komme op. ilden på træpinden slukkede, fordi at der ikke var ilt i bægerglasset, da at den kemiske reaktion i bægerglasset brugte ilt og lavede CO2
2. Vi skulle tage vores andet bægerglas og fylde det op med en halv teske fuld natron og tilføre lidt vand. Derefter målte vi igen ph-værdien og ph-indikatoren viste en grøn farve, dvs at den var basis.
3. Vi har nu vasket glassene og tilført dem tre forskellige stoffer. den tilførte vi 1. citronsyger og sukker med vand. Dette bægerglas bobler en lillesmule. Den 2. bægerglas fyldte vi med natron og sukker. Dette bægerglas viser ingen kemisk reaktion. det 3. bægerglas fyldte vi med citronsyger og natron. Dette bægerglas boblede kraftigt.
4. Vi har taget et stort bægerglas og tilført dem citronsyre og natron uden vand. pulverne citronsyre og natron reagere ikke på hinanden
5. Vi tilføre det stor bægerglas med 50 ml vand og stofferne citronsyre og natron reagere nu kraftigt ved at boble.
Vi sætter nu ild til en træ-pind og prøver at sætte den ned i det store bægerglas. Den slukkede pludseligt da den nærmede sig væsken. Vi prøvede igen, og dette forsøg viste samme resultat. Røgen fra den slukkede træpind forbliver dog i bægerglasset.
Forklaring:
Røgen forbliver i glasset, fordi at den er tungere end luft, og derfor ikke kan komme op. ilden på træpinden slukkede, fordi at der ikke var ilt i bægerglasset, da at den kemiske reaktion i bægerglasset brugte ilt og lavede CO2
forsøg 7.9
i dette forsøg skulle vi først og fremmest bruge et reagensglas stativ hvorpå vi stillede 4 reagensglas, hver fyldt halvt op med vand og vi har hentet 4 balloner til senere. Vi tilsatte forskellige ting til hver af reagensglassene.
0,5 tsk druesukker i glas 1.
0,5 tsk. smuldret gær i glas 2.
0,5 tsk. druesukker og 0,5 tsk. smuldret gær i glas 3
efter tilsætningen af disse stoffer i de første 3 reagensglas har vi rystet glassene for at opløse sukkeret og for at blande gæret med vandet. derefter satte vi en ballon på toppen af de 3 glas, for at lukke ilten og dermed stoppe ydeligere ilttilførelse.
0,5 tsk smuldret gær i glas 4.
glas 4 har vi også rystet glasset efter tilførelsen for at blande vandet og gæret, men derefter også opvarmet reagensglasset indtil det koger, ved at sætte det på et stativ, under en bunsenbrænder. Dette vil gøre at gæren og vandet bliver til en samlet masse. Efter det kogede skulle vi tilsætte 0,5 tsk. druesukker og ryste for at opløse det. Til sidst skulle vi ligesom de andre reagensglas sætte en ballon på toppen.
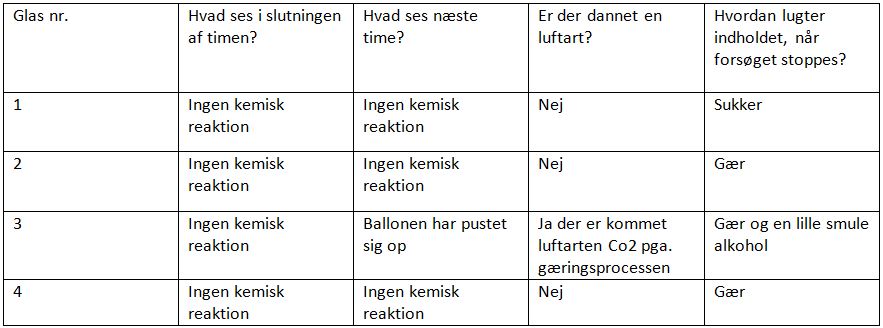
Nogle timer senere begyndte reagensglas nummer 3s ballon at puste sig op. Dog næste dag var ballonen ved at være tømt for luft igen.
Ballonen pustede sig op, fordi at gæren i reagensglasset producerede Co2 da den åd druesukkeret. Dog forsvandt luften senere, fordi den sev
0,5 tsk druesukker i glas 1.
0,5 tsk. smuldret gær i glas 2.
0,5 tsk. druesukker og 0,5 tsk. smuldret gær i glas 3
efter tilsætningen af disse stoffer i de første 3 reagensglas har vi rystet glassene for at opløse sukkeret og for at blande gæret med vandet. derefter satte vi en ballon på toppen af de 3 glas, for at lukke ilten og dermed stoppe ydeligere ilttilførelse.
0,5 tsk smuldret gær i glas 4.
glas 4 har vi også rystet glasset efter tilførelsen for at blande vandet og gæret, men derefter også opvarmet reagensglasset indtil det koger, ved at sætte det på et stativ, under en bunsenbrænder. Dette vil gøre at gæren og vandet bliver til en samlet masse. Efter det kogede skulle vi tilsætte 0,5 tsk. druesukker og ryste for at opløse det. Til sidst skulle vi ligesom de andre reagensglas sætte en ballon på toppen.
Nogle timer senere begyndte reagensglas nummer 3s ballon at puste sig op. Dog næste dag var ballonen ved at være tømt for luft igen.
Ballonen pustede sig op, fordi at gæren i reagensglasset producerede Co2 da den åd druesukkeret. Dog forsvandt luften senere, fordi den sev
forsøg 7.10
Vi har hældt 20 ml vand i et 100 ml bægerglas, og derefter tilført først 0,5 tsk. paprika og derefter 10 dråber sprit. Vi rørte den derefter sammen for at blande vandet og tilsætningsstofferne sammen. Derefter sætter vi et kridt i bægerglasset, som med tape nu sidder fast. Vi venter på at væsken næsten er steget op til toppen af væsken, hvorefter vi prøver at tegne på et kromotografipapiret med kridtet, og vil derefter vente et par dage, for at se om nogle af farverne forbliver derpå. Kridtet viste sig efter 2 dage stadig at have en orange farve og påviser paprikaens ulovlige brug af farvestoffer, som er blevet brugt for at få paprikaen til at se mere indbydende ud. Farvestofferne er ulovlige, fordi farvestoffer kan være kraftfremkaldende.
Da at kridtet i dette forsøg ikke er godt til at absobere væsken, dybbe vi selve kromotografipapiret i væsken.
Dette forsøg kan i hverdagen bruges til at teste tilsættelse af ulovlige farvestoffer i forskellige fødevare-produkter.
Da at kridtet i dette forsøg ikke er godt til at absobere væsken, dybbe vi selve kromotografipapiret i væsken.
Dette forsøg kan i hverdagen bruges til at teste tilsættelse af ulovlige farvestoffer i forskellige fødevare-produkter.
7.10 (smarties)
Fordi at det sidste forsøg med paprikaen ikke viste det tydeligste resultater prøver vi nu det samme med smarties. Vi får farvestofferne omdannet til væske ved hjælp af metoden, som vi brugte i forsøg 7.11 (uden aktivt kul). Dette forsøgs resultat var godt, da at man kunne se vandets farveforandring. Da vi havde gjort dette puttede vi et kromotografipapir direkte i væsken fra starten af, da vi havde fundet ud af at vores kridt ikke var den bedste til at absorbere.
Resultatet viste sig gennem en grønlig gul og brun farve på kromotografipapiret
Resultatet viste sig gennem en grønlig gul og brun farve på kromotografipapiret
Forsøg 7.11
vi har i dette forsøg taget 2 kolber, med 2 tragte og 2 filtrerpapir. i den ene kolbes filtrerpapir har vi tilsat aktivt kulfilter og lidt vand, mens vi i den anden kolbes filtrerpapir ikke har tilsat noget. Derefter har vi så taget et 100 ml bægerglas, tilsæt 4 ensfarvede m&m´s og 50 ml vand og derefter rørt rundt indtil farven er opløst i vandet. vi har nu hældt halvdelen af væsken i den ene kolbe, og resten i den anden kolbe. væsken som kommer igennem filtrerpapiret og tragten viser en meget blå farve i den første kolbe uden det aktive kul. Denne blå farve viser brugen af farvestoffer i m&ms´ene. Den anden kolbe, hvori der er aktivt kul viser dog ikke en blå farve i bunden, men kullet begynder istedet for at få en blålig farve, idet det aktive kul er god til at absorbere.
Aktivt kul: Aktivt kul fremstilles ved delvis oxidation af trækul og andre kulstofholdige materialer med ilt og vanddamp. på grund af dette er kullet velegnet til adsorption af urenheder fra væsker
Aktivt kul: Aktivt kul fremstilles ved delvis oxidation af trækul og andre kulstofholdige materialer med ilt og vanddamp. på grund af dette er kullet velegnet til adsorption af urenheder fra væsker
påvisning af stivelse, protein og fedt i madvarer
Påvisning af stivelse:
Vi startede med at tage 4 forskellige madprodukter. Vi tog en kammerjunke, en riskuks, nogle cerios og nogle choko-flakes
Vi startede med at tage cerios og mase dem hvorefter vi hældte smulleret i et bægerglas med vand derefter hældte vi det i et reagensglas og tilførte benedict-reagens dertil. Derefter så vi på farven, som den gav, og kunne derefter påvise dens stivelse alt efter dens farve. Vi fortsatte ved at gøre direkte det samme ved alle de andre madprodukter, og dette var vores konklusion
Stivelsepåvisningsresultatet:
Cerios: Der var lidt i cerios
Chokoflakes: Der var meget stivelse i chokoflakes
Kammerjunker: Der var lidt stivelse i kammerjunker
Riskiks: der var meget stivelse i riskiks
Konklusion: Det, som vi fandt frem til og faktisk var overrasket over var, at der var mest stivelse i riskiks, selvom vi faktisk troede at der var mest i chokoflakes. Derudover fandt vi frem til at der var mindst stivelse i cerios, som var forventet, da at det er set som et sundt morgenmadsprodukt.
Påvisning af fedt:
Vi tager igen de samme 4 madprodukter, maser dem igen, men denne gang gnider vi dem hen ad et filtrerpapir, som vi derefter kommer lidt vand på og sætter ved radiatoren
fedtpåvisningsresultatet:
Cerios: næsten ingen fedt
kammerjunker: meget fedt
choko-flakes: lidt fedt
riskiks: lift fedt
Påvisningen af sukker 2:
Vi tager igen de samme 4 madvare, maser dem som sædvanligt, og putter dem hver især i hvert deres et reagensglas, blander dem med vand, og tilsætter. Derefter sætter vi reagensglassene i et stort bægerglas med vand i, som står på en trefod, der er placeret under en bunsenbrænder, som vi tænder, og lader koge i 5 minutter.
Proteinpåvisningsresultat: Der er lidt sukker i alle madprodukter
Påvisning af fedtstoffer 2:
Vi har i dette forsøg taget 4 nye madprodukter: abrikos, hamberryg,, chokoflakes og skinke, og puttet dem i et reagensglas. denne gang har vi tilført ethanol (sprit), sat en prop på og rystet dem.
Internettets svar:
Fedt
Kammerjunkere: 17,5%
Choko-flakes
Sukker
Kammerjunkere: 66,4%
Protein
Kammerjunkere: 8,,3%
Vi startede med at tage 4 forskellige madprodukter. Vi tog en kammerjunke, en riskuks, nogle cerios og nogle choko-flakes
Vi startede med at tage cerios og mase dem hvorefter vi hældte smulleret i et bægerglas med vand derefter hældte vi det i et reagensglas og tilførte benedict-reagens dertil. Derefter så vi på farven, som den gav, og kunne derefter påvise dens stivelse alt efter dens farve. Vi fortsatte ved at gøre direkte det samme ved alle de andre madprodukter, og dette var vores konklusion
Stivelsepåvisningsresultatet:
Cerios: Der var lidt i cerios
Chokoflakes: Der var meget stivelse i chokoflakes
Kammerjunker: Der var lidt stivelse i kammerjunker
Riskiks: der var meget stivelse i riskiks
Konklusion: Det, som vi fandt frem til og faktisk var overrasket over var, at der var mest stivelse i riskiks, selvom vi faktisk troede at der var mest i chokoflakes. Derudover fandt vi frem til at der var mindst stivelse i cerios, som var forventet, da at det er set som et sundt morgenmadsprodukt.
Påvisning af fedt:
Vi tager igen de samme 4 madprodukter, maser dem igen, men denne gang gnider vi dem hen ad et filtrerpapir, som vi derefter kommer lidt vand på og sætter ved radiatoren
fedtpåvisningsresultatet:
Cerios: næsten ingen fedt
kammerjunker: meget fedt
choko-flakes: lidt fedt
riskiks: lift fedt
Påvisningen af sukker 2:
Vi tager igen de samme 4 madvare, maser dem som sædvanligt, og putter dem hver især i hvert deres et reagensglas, blander dem med vand, og tilsætter. Derefter sætter vi reagensglassene i et stort bægerglas med vand i, som står på en trefod, der er placeret under en bunsenbrænder, som vi tænder, og lader koge i 5 minutter.
Proteinpåvisningsresultat: Der er lidt sukker i alle madprodukter
Påvisning af fedtstoffer 2:
Vi har i dette forsøg taget 4 nye madprodukter: abrikos, hamberryg,, chokoflakes og skinke, og puttet dem i et reagensglas. denne gang har vi tilført ethanol (sprit), sat en prop på og rystet dem.
Internettets svar:
Fedt
Kammerjunkere: 17,5%
Choko-flakes
Sukker
Kammerjunkere: 66,4%
Protein
Kammerjunkere: 8,,3%
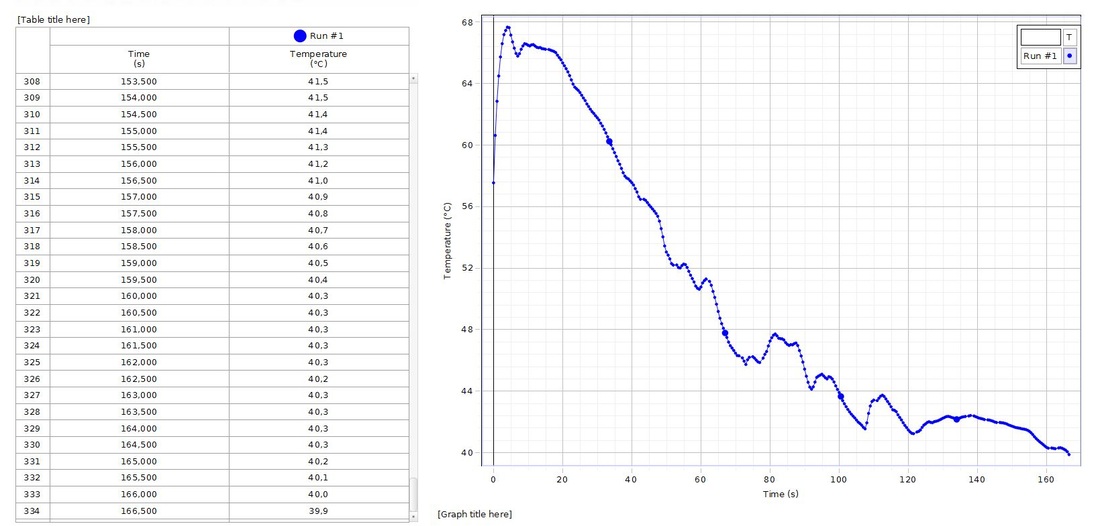
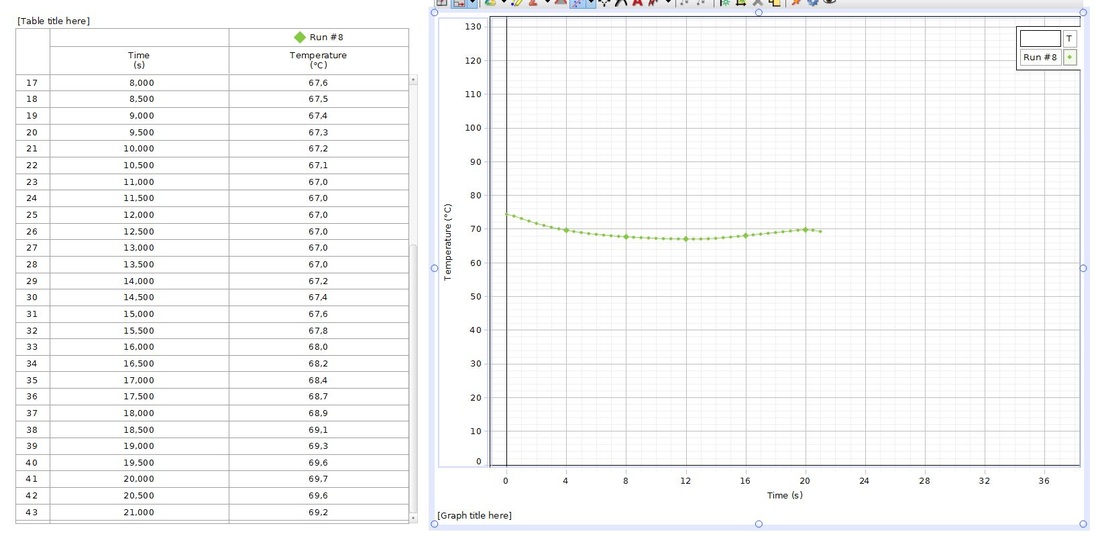
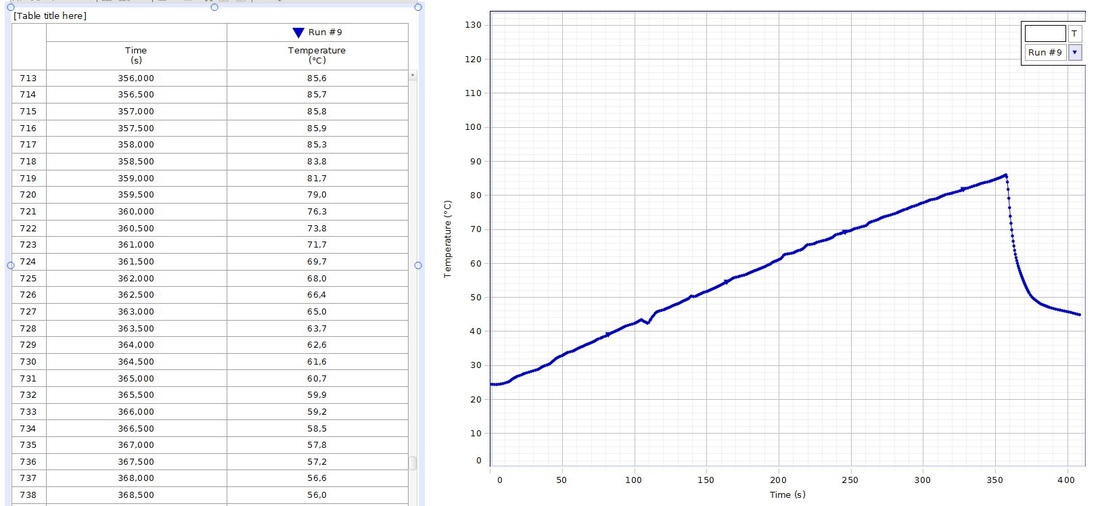
forsøg 7.13
I dette forsøg startede vi med at sætte et stort bægerglas, der er halvt fyldt med vand, op på et keramisk trådnet på en trefod, med en bunsenbrænder under. Imens den varmer op tager vi en kolbe, og putter 10 gram sukker og 10 gram gær i. Derefter sætter vi en prop på og ved hjælp af to lille cylinderglas og en slange koblede vi den til et reagensglas med vand i. Efter at vandet i bægerglasset har nået vores valgte temperatur (20 grader), hældte vi 100 ml. af vandet i bægerglasset ned i kolben. Derefter sattte vi kolben ned i bægerglasset, hvorefter vi ventede i 5 minutter, imens vi forsøgte at holde den valgte temperatur (20 grader). Derefter vil vi begynde og tælle boblerne, som der kommer pr. minut. Resultatet viste, at det ikke var ret aktivt ved 20 grader. Dette er også forudsigeligt, da den bedste temperatur for gæring er ved omkring 37 grader. Dette er fordi at gæren der er på høj nok temperatur til at lave processen og samtidig ikke dø på grund af temperaturen.